|
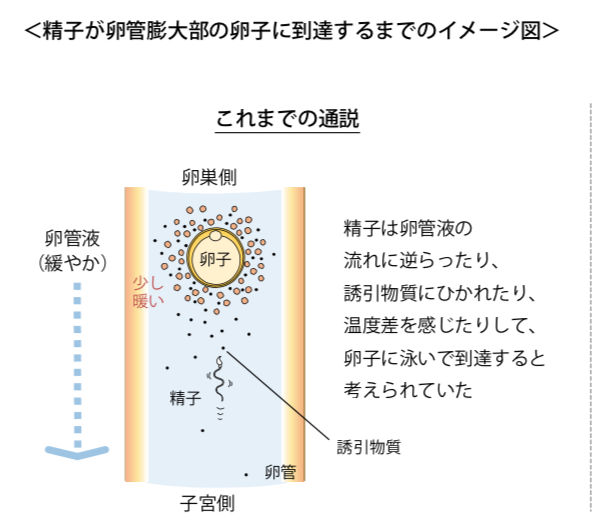
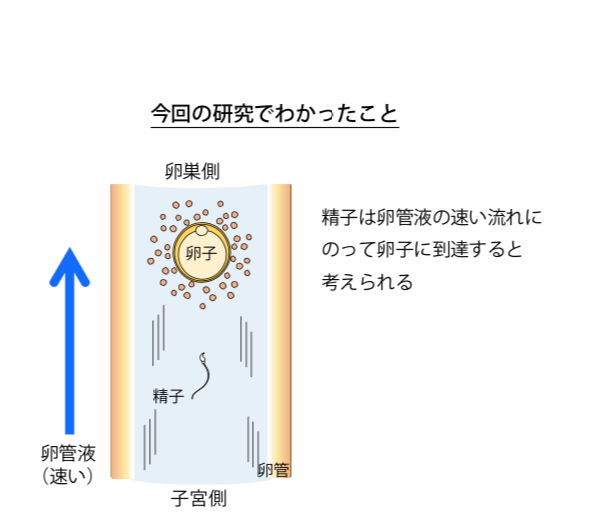
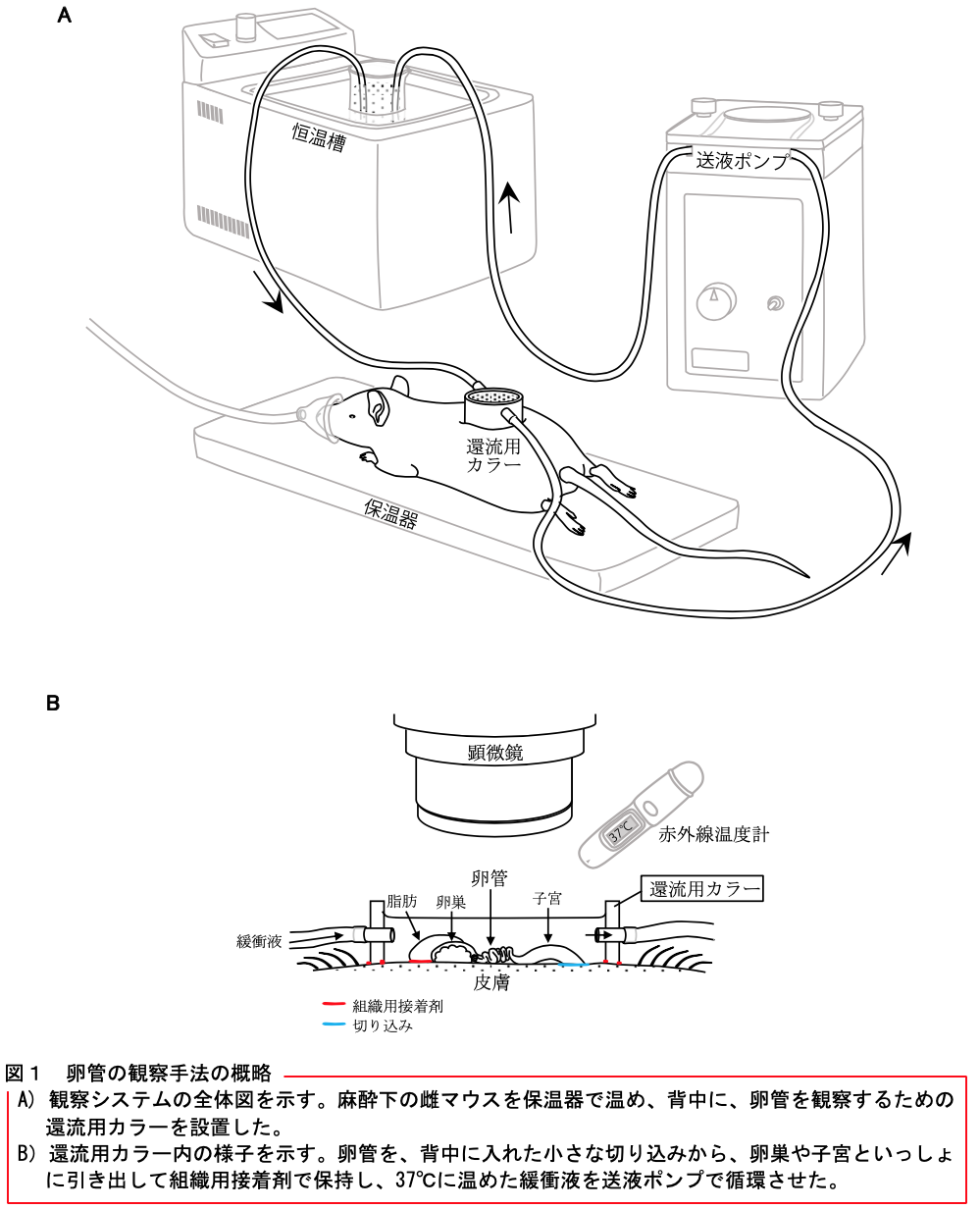
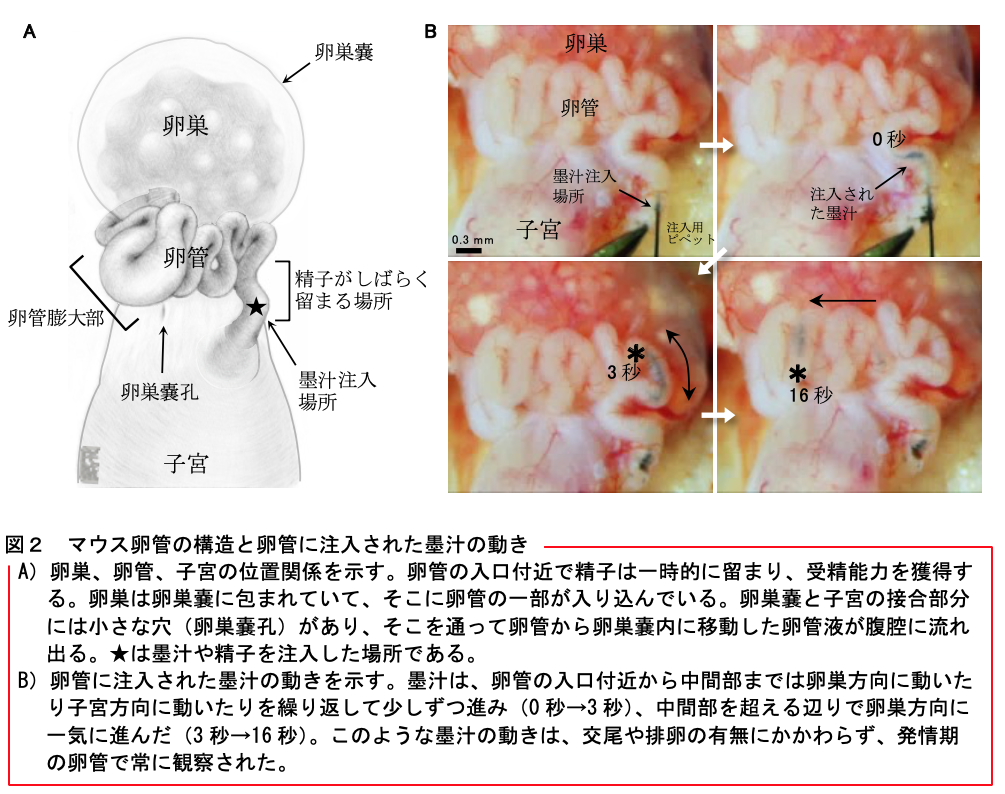
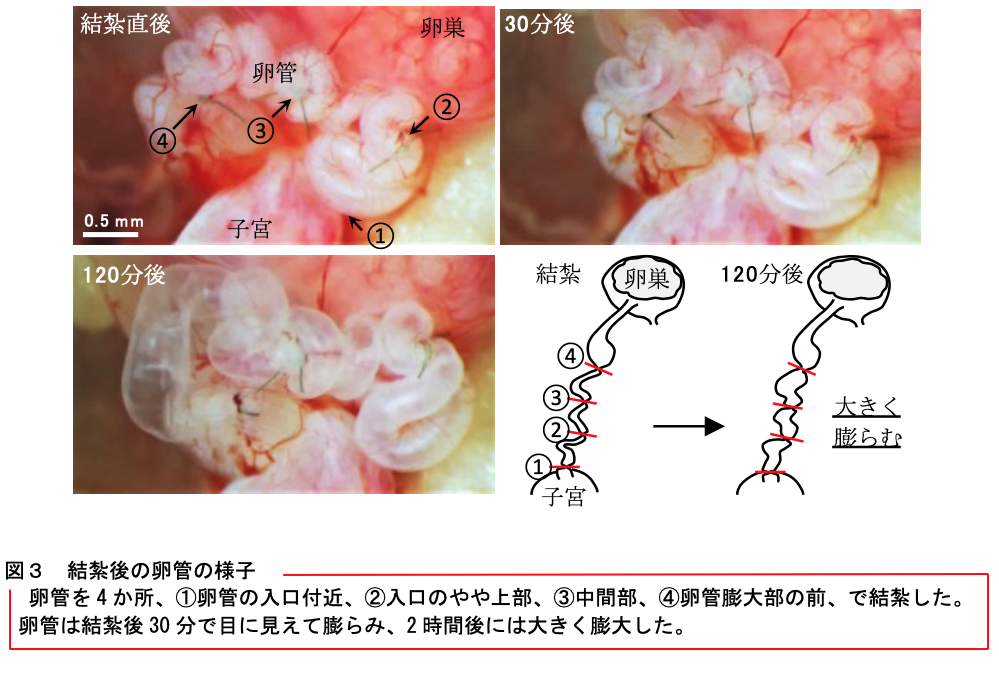
本研究会の会員による論文解説を掲載します。 【タイトル】 マウス卵管の活発な蠕動運動と卵管液の分泌:卵管液や精子の輸送ならびに受精との関係 Active peristaltic movements and fluid production of the mouse oviduct: Their roles in fluid and sperm transport and fertilization 【著者】 日野 敏昭1)、柳町 隆造2) 1) 旭川医科大学医学部生物学教室、2) ハワイ大学医学部 【要約】 精子が卵管内をどのように移動して卵子に到達するかについて、これまでの通説では、卵管の中を卵管液が子宮方向に緩やかに流れており、精子はその流れに逆らったり、卵子や卵子を取りまく細胞から放出された精子誘引物質にひかれたり、温度差を感じたりして、卵管膨大部の卵子に泳いで到達するとされてきた(下図左)。しかし、これらの仕組みは卵管を体外に切り離したり、精子を体外に取り出したりして得られた観察結果から推測されたことであり、生体内でも同じ仕組みが働いているかどうかについて十分な検証は行われていなかった。今回の研究では、卵管を体から切り離すことなくできる限り自然な状態で観察する手法を考案し、卵管の動きや卵管液の流れ、精子の移動のようすを観察した。その結果、卵管は卵管液を活発に分泌しており、それが卵管の活発な蠕動運動よって、卵巣方向に速い速度で押し流されていることが明らかになった。精子はこの流れにのって卵管膨大部の卵子に到達していると考えられる(下図右)。 【背景】 卵管は受精と発生が開始する場として大切な器官である。交尾によって雌の体内に送り込まれた精子は、すみやかに子宮を抜けて卵管に入るが、その後しばらくは卵管の入口付近(子宮側)に留まる。数時間後、精子はそこを離れ、排卵された卵子のある卵管膨大部へと向かう。 これまでの通説では、卵管の中を卵管液が子宮方向に緩やかに流れており、精子はその流れの中を泳いで卵管膨大部の卵子のもとへ向かう(走流性)、卵子や卵子を取りまく細胞から放出される精子誘引物質が子宮方向に向かって流れるため、精子はそれにひかれるように卵管膨大部へ向かう(走化性)、または卵管膨大部の温度がわずかに高いため、精子は温かい方へ向かう(走温性)と考えられていた。 このような精子の性質や卵管液の流れは、いずれも卵管を体外に切り離したり、精子を体外に取り出したりして得られた観察結果であり、体内では精子が如何にして卵管膨大部の卵子までたどり着くのかについて調査した研究はなかった。本研究では、実験動物であるマウスをモデルにして、卵管を体から切り離すことなく血流や神経連絡を保ったまま観察する手法を考案し、それを使って卵管の動きや卵管液の流れが精子の移動や受精にどのような影響を及ぼしているのかを調べた。 【研究手法と成果】 1.卵管の動きと卵管液の流れについて マウス卵管の観察システムを図1に示す。まずは卵管液の流れを可視化するために、卵管の入口付近に微量の墨汁を注入した(図2A)。 発情期の卵管は激しく蠕動していたが、その動きを動画撮影して詳しく調べたところ、蠕動の方向は、卵管の入口付近から中間部までは、卵巣方向であったり子宮方向であったりと、不規則な動きをしていた。ところが、卵管膨大部が近くなると卵管は卵巣方向に蠕動するようになった。この蠕動運動に同調して、卵管内の墨汁も卵管の入口付近から中間部までは行ったり来たりの動きを繰り返しながら卵管膨大部に向かって少しずつ進み、中間部を過ぎると一気に卵管膨大部に向かって移動した(図2B、別ウインドウで動画を開きます)。墨汁は平均して30秒以内に1.2cm先の卵管膨大部まで達した。速さに換算すると毎秒400μm以上となり、実に、精子が泳ぐ速度の2倍以上だった。 2.卵管液の由来について 卵管の入口付近に注入した墨汁は、卵管を通って卵巣嚢に入り、最終的に卵巣嚢孔から腹腔へ流れ出た。ところが、子宮に注入した墨汁は卵管へ移動しなかった。この結果から卵管液は子宮から分泌されたものではないことがわかった。そこで、卵管のいろいろな部位を結紮して卵管液の流れを妨げてみた。すると、どの部位で結紮しても卵管は大きく膨らむことがわかった(図3)。 3.卵管の動きや卵管液の流れと受精の関係について 遺伝子操作で光るように改変された精子を卵管の入口辺りに注入して精子の行動を追跡した。生きた精子は卵管膨大部に到達し、ほぼすべての卵子が受精した。一方、死んだ精子は卵子と受精しなかったが、生きた精子と同じように卵管膨大部に到達した。薬品を使って卵管の動きを止めたり、卵管の出口を結紮して卵管液の流れを止めたりすると、生きた精子であっても、卵管膨大部への移動が妨げられ、受精は大きく抑えられた。 以上から、卵管内には卵管液が常に分泌されており、その液が卵管の蠕動によって卵巣方向に押し流され、その流れが精子を卵管膨大部の卵子へと運んでいることが示された。 【今後の課題と展望】 今回マウスで発見された仕組みが、ヒトを含めたその他の哺乳類に広く共通しているかどうかを調査することで、哺乳類における体内受精の過程の理解がより一層深まると考えられる。また、将来的には不妊症の原因解明や、新たな不妊治療法の開発をも視野に入れた生殖医学の研究につながっていくものと期待される。 【原著論文情報】 Hino T and Yanagimachi R, Active peristaltic movements and fluid production of the mouse oviduct: Their roles in fluid and sperm transport and fertilization, Biology of Reproduction, 2019, DOI: 10.1093/biolre/ioz061, https://doi.org/10.1093/biolre/ioz061 *ここをクリックし別ウインドウで動画を再生します*
0 コメント
本研究会の会員による論文解説を掲載します。 【タイトル】ジメチルスルホキシド(DMSO)及びケルセチンの添加でマウス冷蔵精子の受精能力を10日間維持することに成功 【出展】Dimethyl sulfoxide and quercetin prolong the survival, motility, and fertility of cold-stored mouse sperm for 10 days https://academic.oup.com/biolreprod/advance-article/doi/10.1093/biolre/iox14 4/4604773 Phys.orgでビデオを見る https://phys.org/news/2017-12-refrigeration-technology-cold-stored-mouse-sperm.html
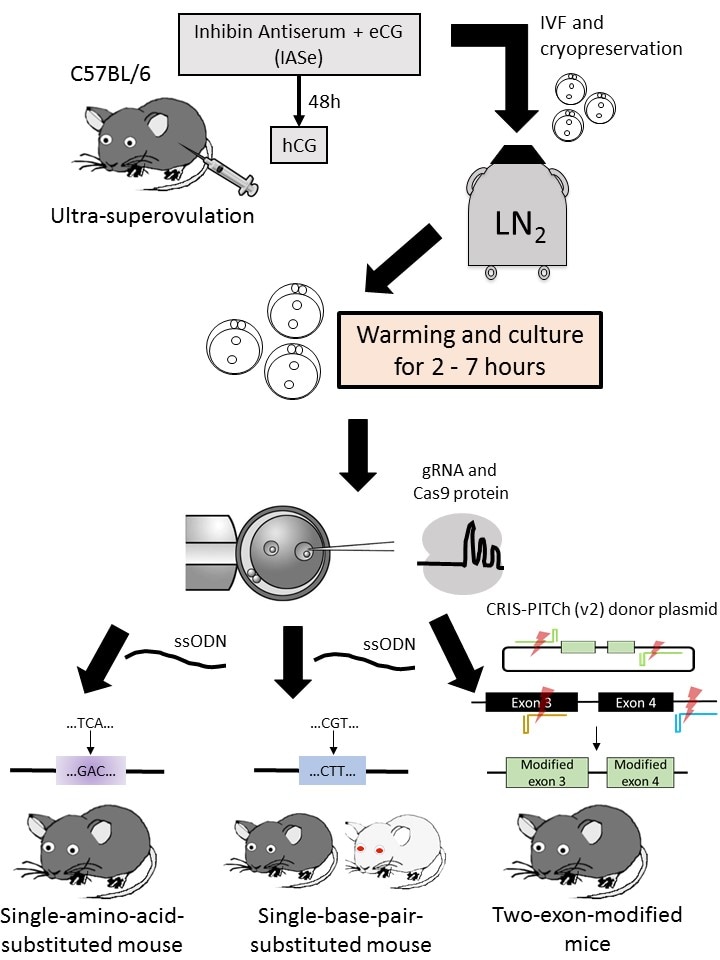
本研究会の会員による論文解説を掲載します。 【タイトル】CRISPR-Casシステムを用いたノックインマウス作製における凍結受精卵培養時間の検討 【本研究の概略】従来の過剰排卵誘起法に比べ、雌マウス1匹からより多くの採卵が可能な超過剰排卵誘起法を用いて体外受精を行い、前核期受精卵を凍結保存した。実験計画に合わせて必要数の凍結受精卵を融解し、2-7時間の培養後、異なるタイミングでマイクロインジェクションを行い、CRISPR-Casシステムと1本鎖オリゴヌクレオチドあるいはPITCh (Precise Integration into Target Chromosome) システムを利用した3種類のノックインマウス作製を試みた。マイクロインジェクションを行うまでの受精卵の培養時間を変えることにより、ノックインマウスの作製効率に差異が生じた。そのため、本研究はノックインマウスを作製する際の有用な知見を提供できると考える。 【著者】中川佳子1、佐久間哲史2、西道教尚3、横崎恭之3、竹尾透1、中潟直己1、山本卓2 1熊本大学生命資源研究・支援センター 動物資源開発研究施設(CARD)資源開発分野 2広島大学大学院理学研究科 数理分子生命理学専攻 分子遺伝学研究室 3広島大学保健管理センター インテグリン治療開発フロンティア研究室 【内容】近年、急速に開発が進んでいるゲノム編集技術をマウス受精卵へ応用することにより、遺伝子改変マウスの作製期間は大幅に短縮されつつある。私達は、超過剰排卵誘起法、体外受精、受精卵の凍結保存などの生殖工学技術とゲノム編集技術を活用した遺伝子改変マウスの作製を目的とし、これまでに体外受精由来の凍結受精卵を用いてTALENやCRISPR-Casシステムによる効率的なゲノム編集個体の作製が可能であることを報告した(Nakagawa et al., 2014, 2015, 2016)。しかしながら、ノックインマウスの作製効率は、ノックアウトマウスの作製効率ほど高率ではなく、ノックインマウスの作製効率を改善することは主要な課題であった。そこで、本研究では、凍結受精卵の融解後の培養時間が、CRISPR-Casシステムと1本鎖オリゴヌクレオチドおよびPITChシステムを用いたノックインマウス作製効率に及ぼす影響について調べた。体外受精後、凍結保存した受精卵を融解、2-7時間培養後、異なるタイミングでマイクロインジェクションを行い、ノックインマウスの作製効率が異なるか否かを検討した。1本鎖オリゴヌクレオチドを用いたノックインマウス作製では、全ての実験区においてノックインマウスを作製することが可能であったが、短時間と長時間培養において、得られた産子のうちノックインマウスの割合が高くなる傾向が見られた。一方、PITChシステムを用いたノックインマウス作製では、短時間培養においてのみ目的とするノックインマウスを作製することができた。今回の報告では、融解後の培養時間が産子への発生率に影響を与えることも示唆されたため、本研究が、目的や個体作製方法の違いによってマイクロインジェクションを行うタイミングを考慮し、より効率的な遺伝子改変マウス作製を行うための一助となれば幸いである。 【出典】Culture time of vitrified/warmed zygotes before microinjection affects the production efficiency of CRISPR-Cas9-mediated knock-in mice. Nakagawa Y, Sakuma T, Nishimichi N, Yokosaki Y, Takeo T, Nakagata N, Yamamoto T. Biol Open. 2017; 6(5):706-713. doi: 10.1242/bio.025122. URL: http://bio.biologists.org/content/6/5/706.long
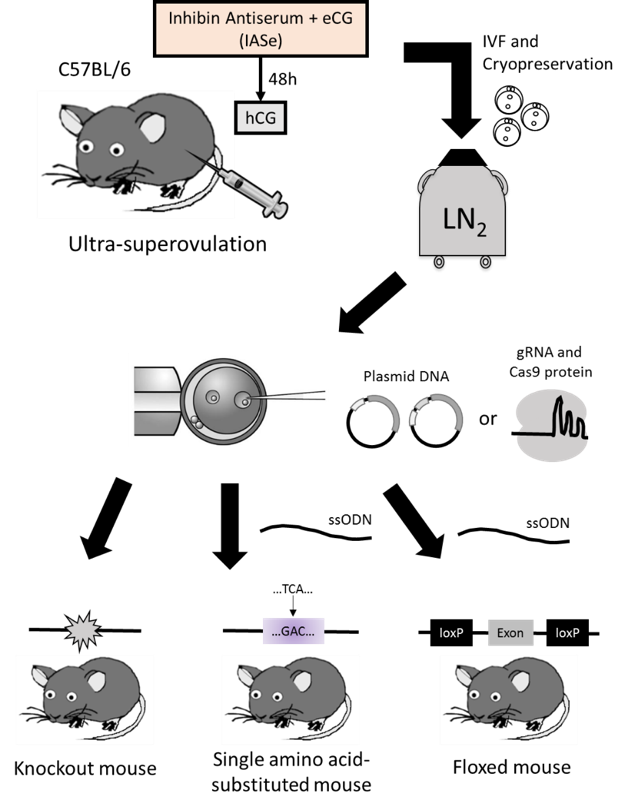
本研究会の会員による論文解説を掲載します。 【タイトル】CRISPR-Casシステムによる様々なゲノム編集個体の作製-超過剰排卵誘起法を用いた体外受精凍結卵の利用- 【本研究の概略】従来の過剰排卵誘起法に比べ、雌マウス1匹からより多くの採卵が可能な超過剰排卵誘起法を用いて体外受精を行い、前核期受精卵を凍結保存した。実験計画に合わせて必要数の受精卵を準備し、gRNAとCas9を発現するプラスミドDNAあるいは合成gRNAとCas9タンパク質をマイクロインジェクションし、ゲノム編集個体を作製した。1アミノ酸置換マウス、Floxマウスの作製にはCRISPR-Casシステムと共に1本鎖オリゴヌクレオチドを使用した。 【著者】中川佳子1、佐久間哲史2、西道教尚3、横崎恭之3,4、矢中規之5、竹尾透1、中潟直己1、山本卓2 1熊本大学生命資源研究・支援センター 動物資源開発研究施設(CARD)資源開発分野 2広島大学大学院理学研究科 数理分子生命理学専攻 分子遺伝学研究室 3広島大学保健管理センター インテグリン治療開発フロンティア研究室 4広島大学大学院生物圏科学研究科 生物機能開発学専攻 分子栄養学研究室 【内容】近年、急速に開発が進んでいるゲノム編集技術をマウス受精卵へ応用することにより、遺伝子改変マウスの作製期間は大幅に短縮されつつある。私達は、体外受精や受精卵の凍結保存などの生殖工学技術とゲノム編集技術を活用した遺伝子改変マウスの作製を目的とし、これまでに体外受精由来の凍結受精卵を用いてTALENやCRISPR-Casシステムによる効率的な遺伝子破壊マウスの作製が可能であることを報告した(Nakagawa et al., 2014、2015)。さらに、インヒビン抗血清とウマ絨毛性ゴナドトロピン(eCG)を同時投与することにより、1匹の雌マウスからより多くの卵を採取することが可能な超過剰排卵誘起法を開発したが(Takeo and Nakagata, 2015)、超過剰排卵誘起法を用いた体外受精由来の凍結受精卵をマイクロインジェクションに使用した場合も、これまで同様、ゲノム編集個体を作製することが可能か否かは明らかとなっていなかった。そのため、従来の過剰排卵誘起法(eCG-hCG)あるいは当研究室で開発した超過剰排卵誘起法(IASe-hCG)を用いて体外受精を行い、得られた凍結受精卵を用いて3種類のゲノム編集個体の作製を試みた。その結果、超過剰排卵誘起法を用いた体外受精卵の発生率や産子における標的遺伝子への変異導入効率は、従来の過剰排卵誘起法を用いた体外受精卵の発生率および変異導入効率とほぼ同等の成績であり、超過剰排卵誘起法を用いた体外受精卵を用いて、1本鎖オリゴヌクレオチドを利用したノックインマウスを作製することも可能であった。また、マイクロインジェクションをgRNAとCas9を発現するプラスミドDNAから合成gRNAとCas9タンパク質を使用する方法へ変更することにより、産子への発生率が改善され、ゲノム編集個体の作製効率を上昇させられることも明らかとなった。超過剰排卵誘起法を用いた体外受精由来の凍結受精卵は、従来法を用いた体外受精由来の凍結受精卵と同様、ゲノム編集個体の作製に十分利用可能であり、今後、多くのゲノム編集個体を作製していく上で、実験動物の福祉や受精卵作製の作業効率化において有用な方法である。 【出典】Ultra-superovulation for the CRISPR-Cas9-mediated production of gene-knockout, single-amino-acid-substituted, and floxed mice Yoshiko Nakagawa, Tetsushi Sakuma, Norihisa Nishimichi, Yasuyuki Yokosaki, Noriyuki Yanaka, Toru Takeo, Naomi Nakagata, Takashi Yamamoto Biol Open. 2016; 5 (8):1142-8. doi: 10.1242/bio.019349. URL: http://bio.biologists.org/content/5/8/1142.long
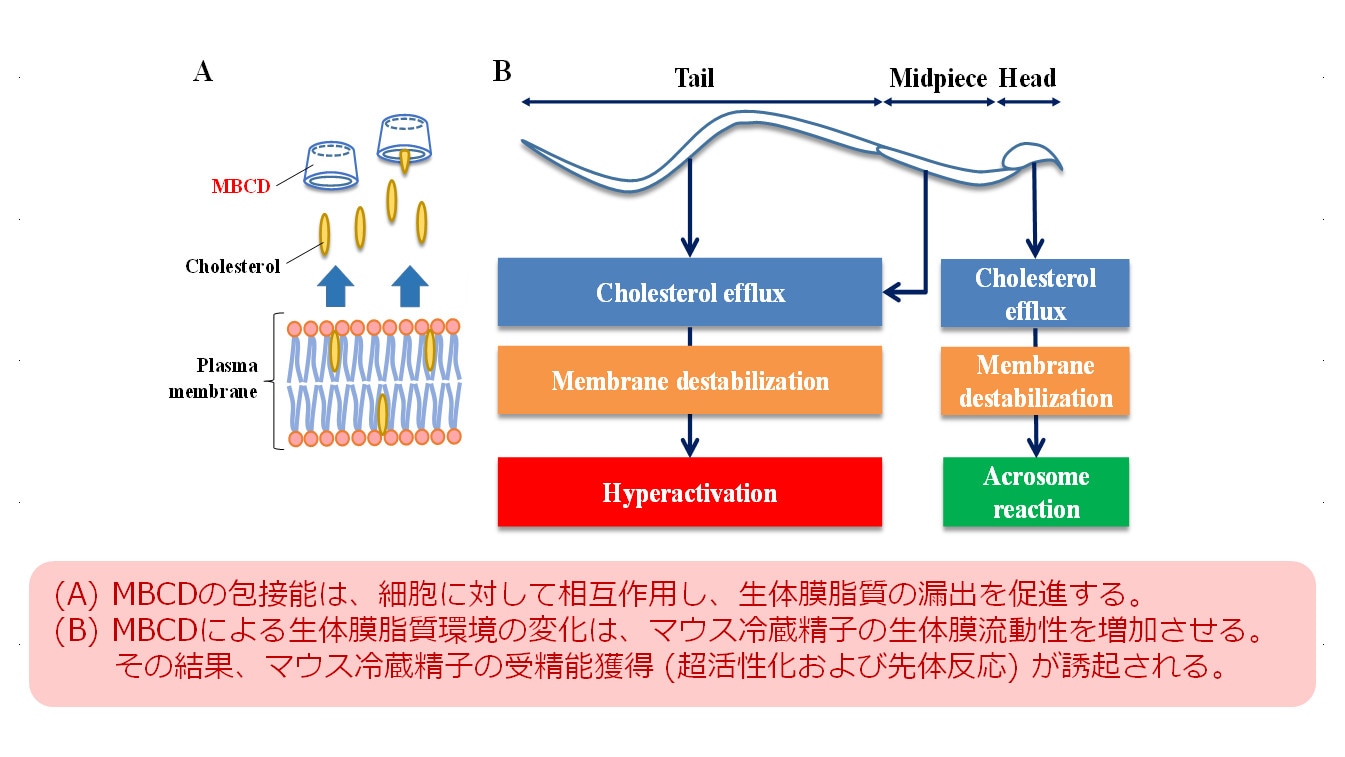
本研究会の会員による論文解説を掲載します。 【タイトル】メチル-β-シクロデキストリン (MBCD) による生体膜脂質環境の変化がマウス冷蔵精子の超活性化を誘起する 【著者】吉本英高1、竹尾 透1、入江徹美2、中潟直己1 1 熊本大学 生命資源研究・支援センター 動物資源開発研究施設 (CARD) 資源開発分野 2 熊本大学 大学院生命科学研究部 薬剤情報分析学分野 【内容】遺伝子改変マウスの輸送には、主に生体による輸送が実施されているが、生体輸送に際して、微生物学的汚染の拡大、輸送中の逃亡や死亡、遺伝子組換え生物の使用に関する法規制および実験動物の福祉の観点から、代替する技術の開発が求められている。そこで我々は、精子の低温保存技術に着目し、遺伝子改変マウスを冷蔵輸送し、輸送された精子を用いた体外受精・胚移植により個体を作製するシステムの構築を試みた。冷蔵保存した精子は、保存期間の延長に伴い受精能の低下が起こるが、メチル-β-シクロデキストリン (MBCD) を処理することで受精能の改善が可能である。しかしながら、マウス冷蔵精子におけるMBCDの受精能改善効果に関する、詳細なメカニズムは不明である。そこで本研究では、MBCDによる受精能改善効果を解明することを目的として、MBCDが冷蔵精子の体外受精率、精子生体膜中コレステロール量、精子先体反応誘起率および精子運動能に及ぼす影響を調べた。その結果、冷蔵精子におけるMBCDの高い受精能改善作用は、強力なコレステロールの除去能が関与していることが示唆された。さらに、MBCDによる精子生体膜中コレステロールの除去は、冷蔵精子における受精能獲得 (超活性化および先体反応) の誘起に密接に関わっている可能性が示唆された。 【出典】 Fertility of cold-stored mouse sperm is recovered by promoting acrosome reaction and hyperactivation after cholesterol efflux by methyl-β-cyclodextrin Hidetaka Yoshimoto Toru Takeo Tetsumi Irie Naomi Nakagata Biol Reprod bio142901. DOI: https://doi.org/10.1095/biolreprod.116.142901 URL: https://academic.oup.com/biolreprod/article/2948758/Fertility-of-cold-stored-mouse-sperm-is-recovered
|
|||||||||||||||||||||||||||||||

 RSSフィード
RSSフィード
